ADDITIF AUX SOLUTIONS DE PRéservation HYPOTHERMIQUE de greffons
Le nombre annuel de transplantations est globalement en constante augmentation, passant de 4 945 en 2011 à 5 276 en 2021 en France, ne permettant pas malgré tout, de combler l’attente des patients, puisque 26 001 patients étaient en attente d’organe en 20201. Il est à noter que parmi ces personnes plus de 900 sont décédées en 2020, faute de greffons disponibles.
Face à cette pénurie d’organes les autorités réglementaires et sanitaires ont autorisé à prélever des greffons sur des donneurs de plus en plus âgés et sur des donneurs à cœurs arrêtés. Ces organes sont très sensibles au cycle d’ischémie-reperfusion.
Aux USA plus de 115 000 personnes sont en attente d’une transplantation2 tout en sachant qu’une étude a montré que sur 8 800 organes collectés, 540 ont été perdus3.
Lors d’une greffe d’organes « solides », l’organe prélevé est soumis à un arrêt brutal d’apport sanguin (i.e. Ischémie) et donc d’oxygène, nécessaire à sa survie. Il est ensuite placé la plupart du temps dans une solution de préservation à 4°C permettant de diminuer le métabolisme du greffon (Figure 1).
Ces lésions d’ischémie/reperfusion dues au manque d’oxygénation du greffon jouent un rôle important dans le rejet primaire de la greffe par le receveur. Les séquences d’ischémie/reperfusion subies par l’organe sont inévitables et induisent l’activation de différentes voies de signalisation (stress oxydant, inflammation, découplage de la chaîne respiratoire mitochondriale) responsables de dommages souvent irréversibles pouvant mener à un rejet précoce ou à une défaillance chronique de l’organe greffé.
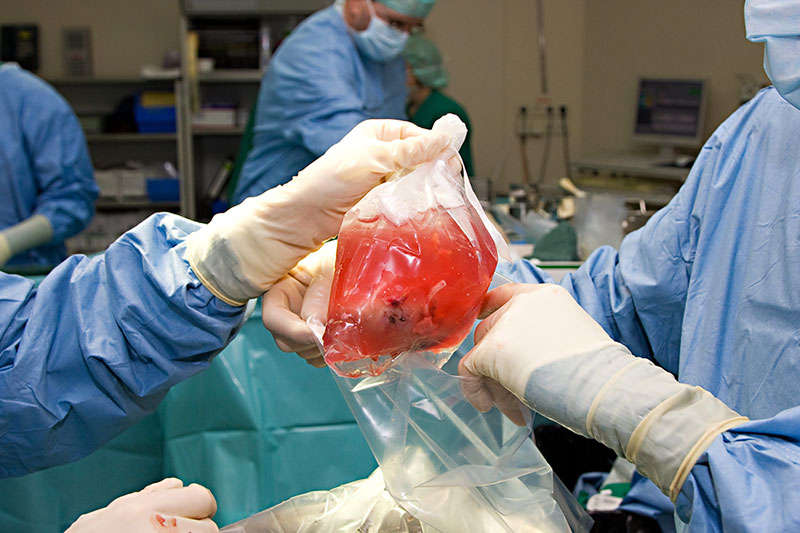


Le challenge est donc majeur pour fournir des solutions permettant de limiter ces lésions et ainsi améliorer la qualité des greffons.
Dans ce contexte, le dispositif médical HEMO2life® développé par Hemarina représente une innovation de rupture majeure dans le domaine de la préservation d’organes. HEMO2life® est un additif à toutes les solutions de préservation d’organes, permettant d’oxygéner le greffon de façon physiologique et donc de considérablement réduire les risques de rejet de la greffe et de prolonger le temps de conservation des greffons.
HEMO2life® a été testé sur plusieurs modèles pré-cliniques, et a fait l’objet de deux études cliniques en transplantation rénale (Oxyop NCT02652520 et Oxyop2 NCT04181710) dirigées par le Pr. Yannick Le Meur (CHRU Brest) et le Pr. Benoît Barrou (APHP, Pitié-Salpêtrière Paris), incluant au total plus de 550 patients.
Une étude rétrospective (Oxyop4 – NCT05050513) a été réalisée afin de suivre les patients de l’étude Oxyop après 4 ans. Le résultat a démontré une meilleure reprise de fonction de l’organe greffé et une meilleure survie des patients ayant reçu un organe conservé avec HEMO2life®.
Une autre étude rétrospective, basée sur la comparaison de données cliniques d’Oxyop et de la base de données ASTRE contenant les paramètres cliniques de 6 584 patients ayant subi une greffe rénale confirment les résultats positifs de l’étude Oxyop et suggèrent que l’amélioration de la reprise de la fonction rénale observée dans le cadre d’Oxyop est clairement liée au bénéfice thérapeutique d’HEMO2life® qui réduit le Delayed Graft Function (DGF) indépendamment du temps d’ischémie froide (Le Meur et al., 2022, Artificial Organ, 46, 597-605).
Depuis 2018, HEMO2life® a également été utilisé à plusieurs reprises dans le cadre de chirurgies réparatrices lourdes et de greffes complexes (greffes de tissus composites).
Le bénéfice immédiat de l’utilisation généralisée de cette technologie serait double : apporter aux chirurgiens transplanteurs des organes en excellentes conditions physiologiques d’une part et d’autre part de leur donner plus de temps entre la collecte du greffon sur le donneur et la transplantation sur le receveur ce qui permettrait de soigner davantage de patients du fait d’une meilleure conservation du greffon en attente de transplantation.
Enfin, grâce à une plus longue conservation possible des organes prélevés, actuellement limitée à quelques heures au-delà desquelles les greffons perdent leurs fonctions métaboliques et leur qualité intrinsèque (de 3 à 4 heures pour un cœur à 24 heures pour un rein) HEMO2life® s’intègre facilement aux pratiques hospitalières actuelles et pourrait faciliter considérablement l’organisation de la greffe en offrant plus de temps au personnel médical dans la préparation de la transplantation.
HEMO2life®est disponible à la vente sur demande.
1. Agence de biomédecine – Données extraites de CRISTAL le 03/03/2021
2. Nombre de candidats à une greffe aux Etats Unis, Organ Procurement & Transplantation Network
https://optn.transplant.hrsa.gov/data/view-data-reports/national-data/#
3. The Organ Shortage Crisis in America , Flescher, Andrew , Washington, DC: Georgetown University Press, 2018.
Dispositif Médical de classe III
HEMO2life® : Publications associées
Asong-Fontem, N., Panisello-Rosello, A., Lopez, A., Imai, K., Zal, F., Delpy, E., Rosello-Catafau, J., Adam, R. A Novel Oxygen Carrier (M101) Attenuates Ischemia-Reperfusion Injuries during Static Cold Storage in Steatotic Livers Int. J. Mol. Sci. - 2021 https://pubmed.ncbi.nlm.nih.gov/34445250/
Ali, A., Watanabe, Y., Galasso, M., Watanabe, T., Chen, M., Fan, E., Brochard, L., Ramadan, K., Ribeiro, RVP., Stansfield, W., Gokhale, H., Gazzalle, A., Waddell, T., Liu, M., Keshavjee, S., Cypel, M. An extracellular oxygen carrier during prolonged pulmonary preservation improves post-transplant lung function J Heart Lung Transplant. - 2020 https://www.ncbi.nlm.nih.gov/pubmed/32334946
Le Meur, Y., Morelon, E., Essig, M., Thierry, A., Büchler, M., Drouin, S., Deruelle, C., Badet, L., Pesteil, F., Delpech, P-O., Boutin, J-M., Renard, F., Barrou, B. First-in-human use of a marine oxygen carrier for organ preservation: a safety and proof-of-principle study. Am J Transplant. - 2020 https://www.ncbi.nlm.nih.gov/pubmed/32012441
Alix, P., Val-Laillet, D., Turlin, B., Ben Mosbah, I., Burel, A., Bobillier, E., Bendavid, C., Delpy, E., Zal, F., Corlu, A., Boudjema, K. Adding the oxygen carrier M101 to a cold-storage solution could be an alternative to HOPE for liver graft preservation. JHEP Rep. - 2020 https://pubmed.ncbi.nlm.nih.gov/32695967/
Lemaire, F., Sigrist, S., Delpy, E., Cherfan, J., Peronet, C., Zal, F., Bouzakri, K., Pinget, M., Maillard, E. Beneficial effects of the novel marine oxygen carrier M101 during cold preservation of rat and human pancreas. Journal of Cellular and Molecular Medicine. - 2019 https://onlinelibrary.wiley.com/doi/full/10.1111/jcmm.14666
Kaminski, J., Hannaert, P., Kasil,A., Thuillier, R., Leize, E., Delpy, E., Steichen, C., Goujon, J.-M., Zal, F., Hauet, T. Efficacy of the natural oxygen transporter HEMO2life® in cold preservation in a preclinical porcine model of donation after cardiac death. Transplant International, official journal of the European Society for Organ Transplantation. - 2019 https://www.ncbi.nlm.nih.gov/pubmed/30924562
Thuillier, R., Delpy, E., Matillon, X., Kaminski J., Kasil, A., Soussi, D., Danion, J., Sauvageon, Y., Rod, X., Donatini, G., Barrou, B., Badet, L., Zal, F., Hauet, T. Preventing acute kidney injury during transplantation: the application of novel oxygen carriers. Expert Opinion on Investigational Drugs, 28(7):643-657. - 2019 https://www.ncbi.nlm.nih.gov/pubmed/31165652
Kasil, A., Giraud, S., Couturier, P., Amiri, A., Danion, J., Donatini, G., Matillon, X., Hauet, T., Badet, L. Individual and combined impact of oxygen and oxygen transporter supplementation during kidney machine preservation in a porcine preclinical kidney transplantation model. International Journal of Molecular Sciences, 20(8). - 2019 https://www.ncbi.nlm.nih.gov/pubmed/31018558
Glorion, M., Polard, V., Favereau, F., Hauet, T., Zal, F., Fadel, E., Sage, E. Prevention of ischemia-reperfusion lung injury during static cold preservation by supplementation of standard preservation solution with HEMO2life® in pig lung transplantation model. Artificial Cells, Nanomedicine, and Biotechnology, 46(8):1773-1780. - 2018 https://www.ncbi.nlm.nih.gov/pubmed/29069926
Ali, A., Watanabe, Y., Galasso, M., Stansfield, W., Watanabe, T., Ramandan, K., Chen, M., Ribeiro, R.P., Gokhale, H., Gazzalle, A., Waddell, T., Liu, M., Keshavjee, S., Cypel, M. Two-Day Lung Preservation Followed by Lung Transplantation in a Large Animal Model Using Novel Extracellular Oxygen Carrier. The Journal of Heart and Lung Transplantation, - 2018 https://www.jhltonline.org/article/S1053-2498(18)30296-1/abstract
Lemaire, F., Bietiger, W., Peronet, C., Langlois, A., Mura, C., Bouzakri, K., Sigrist, S., Polard, V., Zal, F., Pinget, M., and Maillard, E. Effect of HEMO2life®, a marine oxygen carrier, for pancreas preservation during cold ischemia. Poster presented during 8th international EPITA Symposium, Innsbruck, Austria. - 2018
Teh, E. S., Zal, F., Polard, V., Menasché, P., Chambers, D.J. HEMO2life® as a protective additive to Celsior solution for static storage of donor hearts prior to transplantation. Artificial Cells, Nanomedicine, and Biotechnology, 45(4):717-722. - 2017 https://www.ncbi.nlm.nih.gov/pubmed/28079401
Mallet, V., Dutheil, D., Polard, V., Rousselot, M., Leize, E., Hauet, T., Goujon, J.-M., Zal, F. Dose-Ranging study of the performance of the natural oxygen transporter HEMO2life® in organ preservation. Artificials Organs, 38(8):691-701. - 2014 https://www.ncbi.nlm.nih.gov/pubmed/24749976
Zal, F., Rousselot, M. Extracellular Hemoglobins from Annelids, and their Potential Use in Biotechnology Outstanding Marine Molecules, Wiley‐VCH Verlag GmbH & Co. KGaA, - 2014 https://onlinelibrary.wiley.com/doi/abs/10.1002/9783527681501.ch16
Thuillier, R., Dutheil, D., Trieu, M.T.N., Mallet, V., Allain, G., Rousselot, M., Denizot, M., Goujon J.-M., Zal, F., Hauet, T. Supplementation with a new therapeutic oxygen carrier reduces chronic fibrosis and organ dysfunction in kidney static preservation. American Journal of Transplantation, 11(9):1845-1860. - 2011 https://www.ncbi.nlm.nih.gov/pubmed/21875432
Le Meur, Y., Delpy, E., Renard, F., Hauet, T., Badet, L., Rerolle, JP., Thierry, A., Büchler, M., Zal, F., Barrou, B. HEMO2life® improves renal function independent of cold ischemia time in kidney recipients: A comparison with a large multicenter prospective cohort study Artificial Organs. - 2021 https://pubmed.ncbi.nlm.nih.gov/34951495/
Derniers communiqués de presse
Hemarina au service des blessés et de la chirurgie reconstructrice avec le dispositif médical HEMO2life®
Lors de sa visite le 28 avril à l’hôpital militaire Percy, le Président de la République a rencontré plusieurs soldats
L’Institut Amrita des Sciences Médicales (AIMS) de Kochi en Inde devient le premier hôpital au monde à mener une double greffe des membres supérieurs à l’aide de HEMO2life®
Le dispositif médical HEMO2life® contenant un transporteur d’oxygène issu du ver marin arénicole de la société Hemarina, facilitant la conservation
HEMARINA ET LE CHRU DE BREST : L’ESSAI CLINIQUE OXYOP2 DESTINE A EVALUER L’EFFICACITE DU TRANSPORTEUR UNIVERSEL D’OXYGENE HEMO2LIFE® DANS LA GREFFE RENALE SE POURSUIT AVEC SUCCES DANS L’ENSEMBLE DES CENTRES DE TRANSPLANTATION FRANÇAIS
Morlaix, Brest, le 26 novembre 2020 – Le CHRU de Brest et Hemarina, entreprise de biotechnologie bretonne, annoncent aujourd’hui avoir franchi la
CORONAVIRUS : LA MOLECULE D’HEMARINA PEUT SAUVER DES VIES EN REMPLACANT LES RESPIRATEURS ARTIFICIELS POUR OXYGENER DES PATIENTS ATTEINTS DE COVID-19
Morlaix, Bretagne le 19 mars 2020 – J+3 du Confinement – Hemarina, entreprise de biotechnologie bretonne, est prête à mettre
HEMARINA ET DELPHARM ANNONCENT LA SIGNATURE D’UN PARTENARIAT POUR LA FABRICATION D’HEMO2life®
Morlaix et Boulogne-Billancourt (France), le 29 novembre 2018 Hemarina et Delpharm annoncent aujourd’hui avoir conclu un partenariat pour la fabrication
Autres communiqués
Le CHRU de Brest et HEMARINA présentent les nouvelles avancées positives du premier essai clinique d’HEMO2life® au Congrès américain de transplantation de Seattle
6 juin 2018
TÉLÉCHARGER LE COMMUNIQUÉ DE PRESSE
Hemarina et l’University Health Network de Toronto annoncent des résultats positifs de preuve de concept préclinique du transporteur d’oxygène HEMO2life® dans la préservation des greffons pulmonaires avant transplantation
12 avril 2018
TÉLÉCHARGER LE COMMUNIQUÉ DE PRESSE
Le CHRU de Brest et HEMARINA annoncent des résultats positifs du premier essai clinique d’HEMO2life® dans la conservation du rein avant la transplantation chez l’homme.
14 novembre 2017

